石药创新制药子公司SYS6040抗体偶联药物获美国FDA临床试验批准
(原标题:石药创新制药子公司SYS6040抗体偶联药物获美国FDA临床试验批准)
图片来源于网络,如有侵权,请联系删除
中访网数据 石药创新制药股份有限公司(证券代码:300765,证券简称:新诺威)今日公告,其控股子公司石药集团巨石生物制药有限公司研发的注射用SYS6040抗体偶联药物(ADC)已获得美国食品药品监督管理局(FDA)的临床试验批准,将在美国开展针对晚期实体瘤的临床研究。
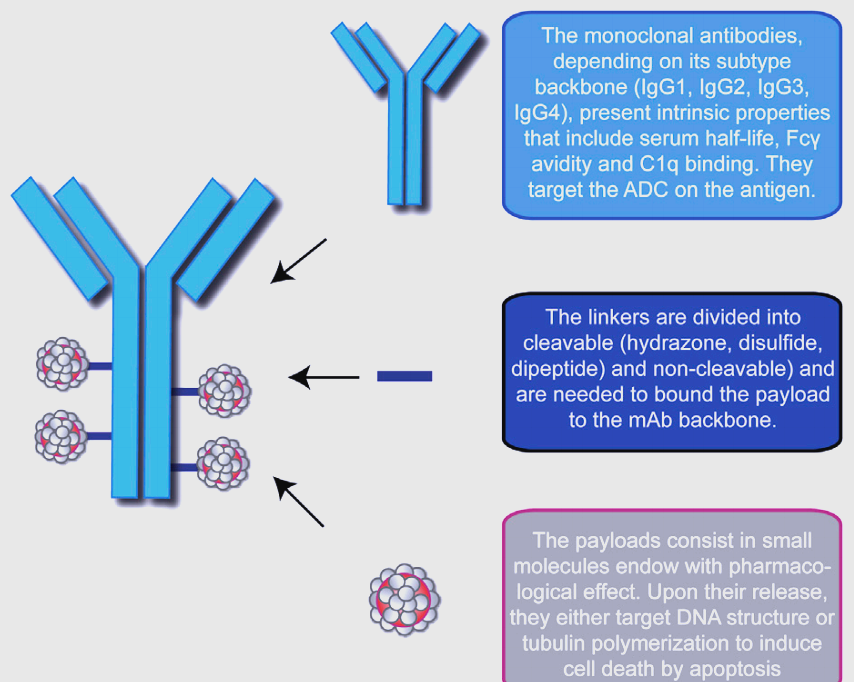
SYS6040是一款通过单克隆抗体靶向肿瘤表面受体的创新药物,通过内吞作用释放毒素杀伤肿瘤细胞。临床前数据显示,该药物对多种癌症具有显著抗肿瘤活性,且已在中美两国提交多项专利申请。此前,该药物已于2025年3月获中国国家药监局批准开展临床试验。
此次获批标志着SYS6040国际化研发进程的重要突破,但公司提示,药物后续仍需完成临床试验并通过FDA审批方可上市,存在研发周期长、效果不及预期等风险,短期内对业绩无直接影响。石药创新表示将根据研发进展及时披露信息,提醒投资者注意风险。
目录 返回
首页
